Validación de software para laboratorios (LIMS, Excel, ERP y sistemas internos)
Asegura que tu software cumple con los requisitos de integridad de datos, trazabilidad y normativa aplicable
(ISO 17025, ISO 15189, GMP o NCF, GDP o BPD) mediante una validación estructurada y documentada.
Reserva reunión gratuita Solicitar propuesta

¿Tu software cumple realmente con los requisitos normativos?
Muchos laboratorios utilizan:
Hojas Excel para cálculos
LIMS sin validar completamente
ERP adaptados internamente
Registros manuales con transcripción
El problema es que:
No hay evidencia de validación
No se controlan los cambios
No se garantiza la integridad de los datos
No se documentan pruebas ni verificaciones
Esto puede derivar en no conformidades durante auditorías.


Validación de software adaptada a la realidad de tu laboratorio
Te ayudo a validar tus sistemas informáticos de forma práctica y conforme a normativa, sin complicar innecesariamente el proceso.
El objetivo es:
Asegurar que el software funciona correctamente
Demostrarlo mediante evidencias documentadas
Cumplir con requisitos de auditoría
Reducir riesgos asociados a datos y cálculos
¿Qué tipo de software se puede validar?
Servicios de Validación de Software
Validación inicial
Para software nuevo o no validado.
Revalidación
Tras cambios, actualizaciones o incidencias.
Evaluación de software existente
Diagnóstico del estado actual, (validación retrospectiva).
Documentación de Validación
Protocolos, informes, registros.
Validación de hojas Excel
Control de fórmulas, bloqueos, versiones y uso.
Cómo se realiza la validación
1
Identificación del software y su uso
2
Análisis de riesgos
3
Definición de requisitos
4
Diseño de pruebas
5
Ejecución y registro de resultados
6
Informe de validación final
Cumplimiento de requisitos normativos (ISO y sector farmacéutico)
La validación de software es un requisito clave en:
ISO/IEC 17025
ISO 15189
GMP / NCF (Normas de Correcta Fabricación)
GDP / BPD (Buenas Prácticas de Distribución)
Requisitos de integridad de datos
Y está directamente relacionada con:
Integridad de datos
Trazabilidad
Seguridad de la información
Fiabilidad de resultados
Enfoque práctico basado en laboratorio
No se trata solo de validar software, sino de entender cómo se utiliza en tu operativa real.
Esto permite:
Adaptar la validación al uso real
Evitar documentación innecesaria
Cumplir requisitos sin sobrecargar procesos
Integrar la validación dentro del sistema de calidad
Servicios de Validación GMP y GDP
Validación completa del ciclo de vida del software según NCF (GMP) y BPD (GDP).
Definición de requisitos (URS)
Elaboración de las Especificaciones de Requisitos de Usuario (URS) adaptadas a tu laboratorio.
Planificación de la validación
Desarrollo del Plan Maestro de Validación (PMV).
Evaluación del software y del proveedor
Análisis del software y revisión documental del proveedor para verificar si cumple los requisitos.
Análisis de riesgos
Identificación de funciones críticas y evaluación del impacto sobre los datos.
Ejecución de la Validación
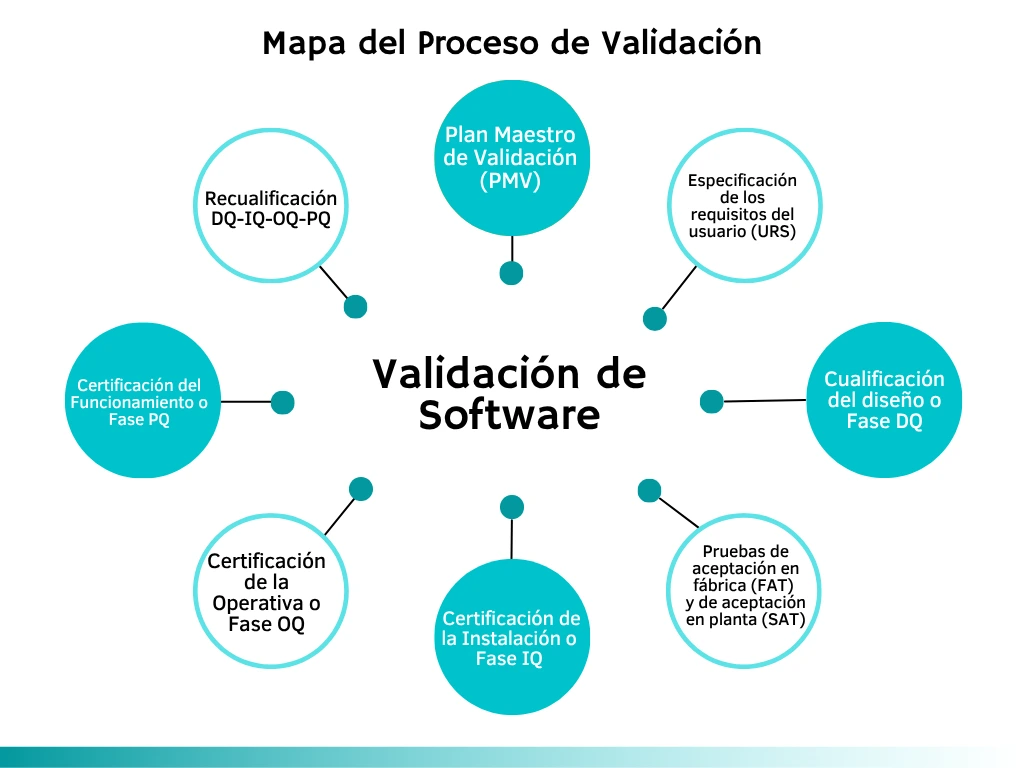
Diseño y ejecución de protocolos de las fases: • DQ (Design Qualification), IQ (Installation Qualification), OQ (Operational Qualification) y PQ (Performance Qualification).
Verificación y documentación
Registro de resultados, desviaciones y evidencias.
Informes de validación
Elaboración de Informes por fases, Informe Final de Validación y toda la documentación para la inspección.
Liberación del sistema
Justificación documentada de que el software es apto para su uso.
control de cambios y revalidación
Gestión de modificaciones y mantenimiento del estado validado.
Un enfoque técnico completo, no solo documental
A diferencia de otros enfoques genéricos, nuestro enfoque incluye:
- Participación desde la definición de requisitos (URS)
- Validación alineada con uso real del laboratorio
- Integración con ISO 17025 / 15189 y GMP
- Experiencia en Excel, LIMS y ERP
Lo que permite que la validación sea útil, defendible en auditoría y aplicable en el día a día.

Qué consigues con la validación de software
Cumplimiento de requisitos normativos
Reducción de riesgos en datos y cálculos
Preparación para auditorías
Mayor control sobre sistemas informáticos
Evidencias documentadas de funcionamiento
Ejemplo de Validación en entorno real: Software ERP
Realizamos la validación de un sistema ERP adaptado a una empresa de distribución cosmética en un entorno regulado según Buenas Prácticas de Distribución (BDP o GDP). Todas las actividades que realizamos fueron:
- Definición de URS
- Evaluación del proveedor
- Análisis de riesgos
- Diseño de pruebas y Ejecución de DQ/IQ/OQ/PQ
- Verificación de todos los procesos a validar
- Documentación completa
Resultado: Sistema validado y preparado para auditoría.

Preguntas frecuentes sobre validación de software
Estas son algunas de las preguntas comunes sobre la validación de software.
Depende del tipo de sistema y normativa aplicable, pero suele ser requerido cuando afecta a resultados.
Sí, cuando se utiliza para cálculos o decisiones críticas.
Cada cuánto hay que revalidar.
Sí, la validación debe quedar documentada.
Nuestro contenido más reciente sobre Validación de Software
Conoce las novedades sobre como validar diferentes tipos de software en tu empresa.
Valida tu software y evita problemas en auditoría
Si utilizas LIMS, Excel, ERP u otros sistemas en tu laboratorio: